Les lignes directrices de l’OMS sur le paludisme sont la principale référence qui guide les politiques nationales de prise en charge du paludisme. La recommandation de nouveaux médicaments repose sur une analyse approfondie et complète des éléments de preuve selon le processus GRADE, qui fournit une approche systématique en vue de formuler des recommandations sur la pratique clinique. À l’issue de cette revue – qui a validé l’une des plus grandes études cliniques visant à évaluer la sécurité et l’efficacité d’un antipaludique en vie réelle – le Comité d’examen des directives a recommandé l’inclusion officielle de Pyramax dans les lignes directrices avec une recommandation « FORTE » – le plus haut niveau d’évidence.
Pyramax est une combinaison thérapeutique à base d’artémisinine (CTA) à dose fixe et la seule à être indiquée pour le traitement au stade sanguin des deux espèces dominantes de parasites du paludisme : P. falciparum et P. vivax.
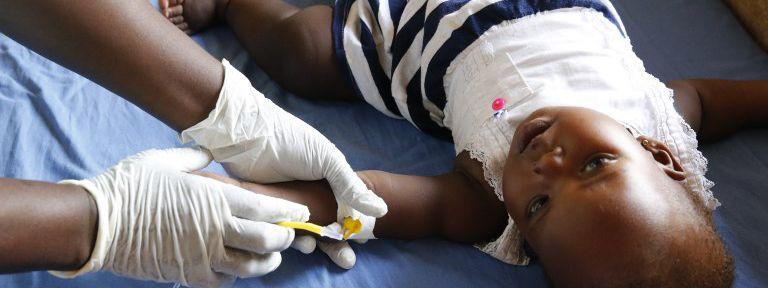
Le médicament est également disponible dans une formulation de granules adaptée aux enfants pour garantir la palpabilité et donc le dosage correct pour cette population vulnérable.
Les comprimés et les granules Pyramax ont reçu des avis scientifiques positifs du comité des médicaments à usage humain (CHMP) de l’Agence Européenne des Médicaments (EMA) au titre de l’article 58, sur la base d’un programme de développement robuste.
A ce jour, plus de 2,9 millions de patients atteints de malaria ont été traités avec ce médicament, y compris des enfants de moins de 1 an.
Les deux formulations sont actuellement enregistrées pour le traitement du paludisme simple dans 29 pays d’Afrique et d’Asie.
Guinee28